Table des matières
Protoxyde d'azote
- “Myelite transverse aiguë toxique de moelle avec des formes de paraplégie laissant souvent des séquelles sensitivo motrices voire des troubles vesico sphinctériens selon le niveau d’atteinte”
- “ça peut même mimer des polyradiculonevrites comme des Guillain barré”
- “Carence en vitamine B12 par toxicité du protoxyde d’azote : une cause méconnue de sclérose combinée de la moelle”
Utilisation grand public : dans les siphons pour crème chantilly, espumas
Usage comme drogue
lien : Detail from a satirical print from 1830 depicting Humphry Davy administering a dose of Laughing Gas to a woman while Count Rumford looks on (cropped out of the picture above), above the caption “Prescription for Scolding Wives”
Vidéo : Le gaz hilarant : la mode qui cartonne chez les ados, Le Parisien, décembre 2018
Transcription : Dans les rues de Lille, des capsules grises et des ballons sont répandues un peu partout dans le centre-ville. Elles contiennent du protoxyde d'azote, autrement dit, du gaz hilarant. Elles sont utilisées pour faire la crème chantilly ou dans les hôpitaux pour anesthésier. Mais surtout, elles sont de plus en plus utilisées par des adolescents et étudiants, qui l’inhalent à l’aide d’un ballon pour ses effets euphorisant. A forte dose, le protoxyde d'azote est dangereux pour la santé, voir mortel.
Un étudiant interrogé : « J'ai l'habitude d'en faire au nouvel an. C'est une sorte de petite tradition avec mes amis. On met chacun à notre tour le gaz hilarant dans un ballon de baudruche, on le ferme bien, on essaye de le faire tous en même temps, comme ça on déconnecte tous en même temps et on rigole tous. On se sent un petit peu comment dire (…) on est très réceptif à la musique, très réceptif à tout ce qui nous entoure, ça procure des fous rires, une espèce de sentiment de bien-être. Au bout d'une ou deux minutes l'effet est parti et on redevient à peu près normal. »
Ce phénomène, au départ pratiqué dans les soirées d'étudiants en médecine, se répand de plus en plus chez les adolescents. À forte dose, le protoxyde d'azote est dangereux pour la santé, voire mortel.
Le Dr. Mourad Benyamina, médecin anesthésiste et réanimateur à l'hôpital Saint-Louis (Paris 10) : « Le protoxyde d'azoté utilisé dans un cadre médical est utilisée associé constamment à l'oxygène. Si vous prenez ce produit, que vous le sortez du cadre médical, il est utilisé, comme en ce moment, dans le cadre festif. Il est utilisé pur et l'effet disparaît très vite. le problème c'est qu'il est réutilisé plusieurs fois parce qu'i est court. Donc quand on le réutilise plusieurs fois dans une soirée, on aboutit à la toxicité et cette toxicité peut aboutir à un arrêt cardiaque. Si vous le prenez, vous pouvez avoir aussi une incoordination de vos mouvements. Donc le protoxyde d'azoté utilisé pour des raisons festives en dehors d'un cadre médical n'est pas anodin et complètement, complètement dangereux, donc il faudra très vite très vite tirer les sonnette d'alarme et en contrôler la consommation. »
Le protoxyde d'azote est légal en France. Il est facile de s'en procurer sur internet ou en supermarché. Selon une étude de la mutuelle étudiante Smerep, publiée en juin 2018, il serait devenu le troisième produit psychoactif le plus consommé chez les étudiants.
- Presse belge
- Presse française :
- Protoxyde d’azote : Bientôt une loi pour interdire la vente de gaz hilarant aux mineurs ?, 20minutes.fr, 09/12/2019
- Tout savoir sur le protoxyde d’azote et les dangers réels de ce gaz hilarant franvetvinfo.fr, 11/09/2019
- tweets :
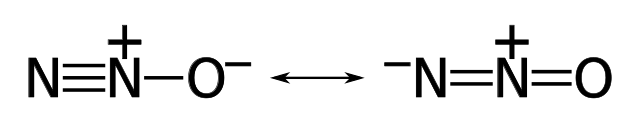
Structure de Lewis
La structure à gauche de la figure (cf. lien) est la plus probable, car la charge formelle négative se trouve sur l'atome le plus électronégatif (O)
- Cf. Méthodologie de détermination du nombre d'oxydation et des formules de Lewis (accès restreint)
- What is the Lewis electron dot formula (Lewis structure) of Nitrous Oxide (N_2O)? Socratic → pourquoi l'atome central n'est pas l'oxygène (N-O-N) → l'atome central est moins électronégatif
Exercice avancé utilisant le moment dipolaire
Sachant que la molécule de protoxyde d'azote, N2O, possède un moment dipolaire µ = 5,6.10-31 Cm, montrer qu'aucune des deux formes de Lewis suivantes de la molécule ne peut rendre compte à elle seule de la valeur de son moment dipolaire.
µ = e d = 1,602.10-19 * 120 10-12 = 1,9 10-29 Cm, très supérieur à la valeur réelle.
Expliquer alors pourquoi, la structure réelle de la molécule est représentée par une superposition des deux formes précédentes.
Données : les longueurs des liaisons dans la molécule sont proches de 120 pm, la charge élémentaire e = 1,602.10-19 C.
µ = a µ1 + b µ2 avec a, b les deux proportions constantes des deux formes

Utilisation dans la crème chantilly

Le N2O est un liquide à pression relativement basse (environ 52 atm). Il est donc possible d'en obtenir plus dans un petit volume qu'avec d'autres gaz comme l'azote. En raison de son excellente solubilité dans les graisses, le N2O est capable de faire mousser la crème fouettée jusqu'à quatre fois le volume liquide d'origine, alors qu'avec l'air ou l'azote, le volume peut seulement être doublé.
le protoxyde d'azote n'est pas toxique, est bactériostatique, et se dissout facilement sous pression dans la crème introduite préalablement dans la bouteille. De nombreuses petites bulles sortent de la solution au fur et à mesure que la crème est expulsée de la bouteille, la gonflant instantanément.
Tout autre gaz propulseur disponible (CO2, propane, fréons) est soit trop toxique pour être utilisé dans les aliments, soit inflammable, soit ne se dissout pas dans la crème de manière équivalente.
- photos de cartouches

Gaz à effet de serre
- A comprehensive quantification of global nitrous oxide sources and sinks Tian, H., Xu, R., Canadell, J.G. et al. Nature 586, 248–256 (2020). DOI: 10.1038/s41586-020-2780-0
Anesthésiant, effets médicaux,...
- Nitrous Oxide and the Inhalation Anesthetics Daniel E Becker, DDS and Morton Rosenberg, DMD, Anesth Prog. 2008 Winter; 55(4): 124–13 DOI: 10.2344/0003-3006-55.4.124
- One month of nitrous oxide abuse causing acute vitamin B 12 deficiency with severe neuropsychiatric symptoms Michael S Lundin, John Cherian, Michael Nyika Andrew and Richa Tikaria, BMJ Case Reports, February 2019 DOI: 10.1136/bcr-2018-228001
- Subacute combined degeneration of the spinal cord following nitrous oxide anesthesia: A systematic review of cases Kishan K.Patel et al, Clinical Neurology and Neurosurgery Volume 173, October 2018, Pages 163-168 DOI: 10.1016/j.clineuro.2018.08.016
- Carence en vitamine B12 par toxicité du protoxyde d’azote : une cause méconnue de sclérose combinée de la moelle C. Chaugny et al, La Revue de Médecine Interne
Volume 35, Issue 5, May 2014, Pages 328-332
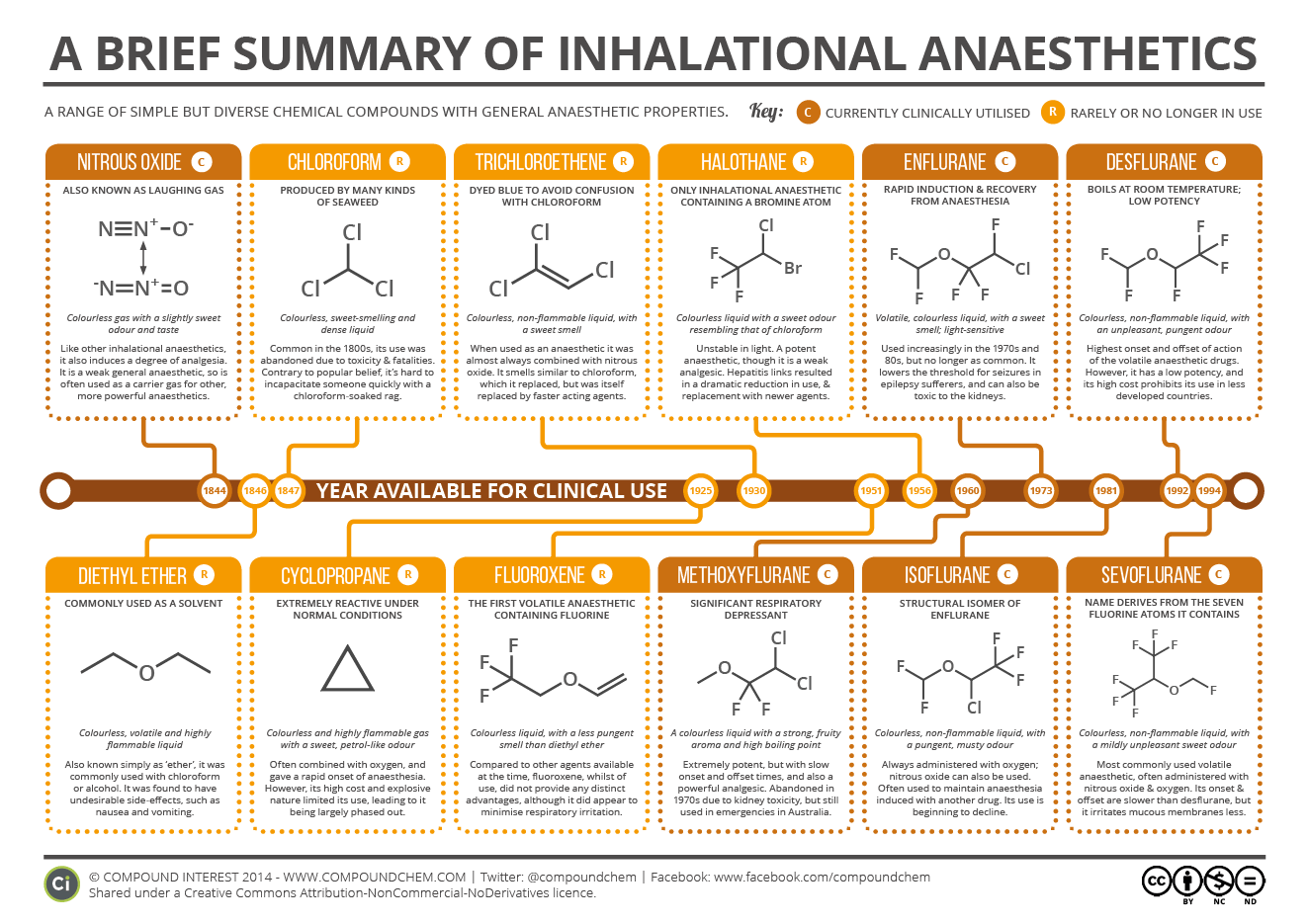
Source image : A Brief Summary of Inhalational Anaesthetics (Compound Interest, 2014, image cc-by-nc-nd)
Histoire
- Joseph Priestley : Le volume I, d'Experiments and Observations on Different Kinds of Air, présente plusieurs découvertes dont le « diminished ou dephlogisticated nitrous air » (protoxyde d'azote, N2O)
- Humphry Davy : On lui doit plusieurs découvertes importantes, entre autres celles des propriétés euphorisantes du protoxyde d'azote (ou « gaz hilarant ») synthétisé par Joseph Priestley.
- cf. recherches avec les mots-clés “Davy nitrous oxide”